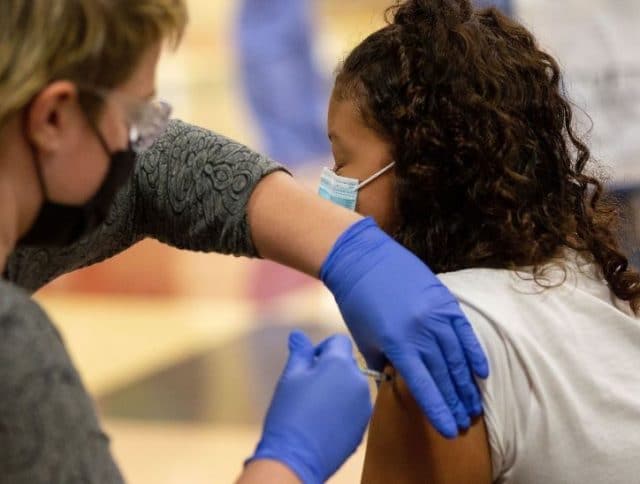
En su plan de combatir la pandemia por coronavirus, Estados Unidos autorizó el 2 de noviembre último aplicar la vacuna de Pfizer contra COVID-19 a niños de 5 a 11 años. La directora de los Centros para el Control y la Prevención de Enfermedades (CDC, en inglés) de Estados Unidos, Rochelle Walensky, autorizó que la vacuna contra la COVID-19 de Pfizer-BioNTech se administre a menores de entre 5 y 11 años, población que se estima en unos 28 millones de niños.
De acuerdo con datos de los CDC, desde el comienzo de la pandemia se han registrado 1,9 millones de casos de COVID-19 entre menores de entre 5 y 11 años, 8.300 hospitalizaciones y 94 muertes. La vacuna de Pfizer-BioNTech para los niños de entre 5 y 11 años -que será de 10 miligramos, un tercio del suero de los adultos- no es administrada en grandes centros de inmunización, sino en clínicas pediátricas y farmacias.
En el primer estudio científico publicado en una revista internacional en el que se hace una revisión de la vacuna Pfizer aplicada en menores, se encontró que “un régimen de vacunación contra Covid-19 que consiste en dos dosis de 10 μg administradas con 21 días de diferencia es seguro, inmunogénico y eficaz en niños de 5 a 11 años de edad”.
La vacuna BNT162b2 recibió la autorización de uso de emergencia de la Administración de Alimentos y Medicamentos (FDA) en diciembre de 2020 para la prevención de la enfermedad por coronavirus 2019 (Covid-19) en personas de 16 años o más, con la posterior expansión a 12 a 15 de 5 a 11 años el 29 de octubre de 2021, sobre la base de los datos de este ensayo.
“Los resultados del estudio clínico de fase I–II–III en curso en personas sanas de 12 años de edad o más, respaldan la seguridad, inmunogenicidad y eficacia de una serie de dos dosis de 30 μg de inyecciones de Pfizer (BNT162b2) administradas con 21 días de diferencia. Se ha demostrado que la vacuna tiene un perfil de seguridad aceptable caracterizado por dolor transitorio leve a moderado en el lugar de la inyección, fatiga y dolor de cabeza, fue más inmunogénico entre los jóvenes de 12 a 15 años que entre los adultos jóvenes, y fue del 95 al 100% eficaz para prevenir la enfermedad por COVID-19 desde 7 días hasta aproximadamente 2 meses después de la segunda dosis”, asegura el informe publicado en JAMA.
En el estudio se advierte que aunque COVID-19 es generalmente más leve en niños que en adultos, pueden ocurrir enfermedades graves y complicaciones a largo plazo, incluido el síndrome inflamatorio multisistémico en niños (MIS-C), después de la infección primaria. “Los niños en edad escolar representan una alta proporción de casos de Covid-19, y pueden desempeñar un papel importante en la transmisión del SARS-CoV-2, incluida la propagación de la variante delta. A fines de septiembre de 2021, las personas menores de 18 años representaban más de una cuarta parte de los casos semanales en EEUU y del 1,6 al 4,2% de las hospitalizaciones acumuladas.
También destaca que las hospitalizaciones de niños asociadas a COVID-19 han aumentado de manera constante desde principios de julio de 2021 en los Estados Unidos. La prevalencia entre los niños de 5 a 11 años alcanzó un máximo histórico de 1,1 por 100.000 habitantes a finales de septiembre. “La pandemia también ha interrumpido la educación y ha afectado negativamente el desarrollo social y emocional y la salud mental de los niños. Por lo tanto, la disponibilidad de vacunas seguras y eficaces para los niños en edad escolar es fundamental”, indica el estudio.
Metodología
En el ensayo de fase II-III, se asignó al azar a un total de 2268 niños para recibir la vacuna BNT162b2 (1517 niños) o placebo (751 niños). En el punto de corte de los datos, la mediana de seguimiento fue de 2,3 meses. En los niños de 5 a 11 años, como en otros grupos de edad, la vacuna de Pfizer tuvo un perfil de seguridad favorable. No se observaron eventos adversos graves relacionados con la vacuna. Un mes después de la segunda dosis, la proporción media geométrica de los títulos neutralizantes del coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) en niños de 5 a 11 años y los de 16 a 25 años fue 1.04, una proporción que cumple el criterio de éxito de inmunogenicidad preespecificado. También se informó del contagio de COVID-19 con inicio 7 días o más después de la segunda dosis en tres menores vacunados y en 16 receptores de placebo.
La mayoría de las reacciones locales fueron de leves a moderadas y todas fueron transitorias (Fig. S1A y Tabla S4). La fiebre fue más común en el grupo de dosis de 30 μg que en los grupos de dosis de 10 μg y 20 μg después de la primera y segunda dosis (Fig. S1B). Los cuatro participantes centinela en el grupo de nivel de dosis de 30 μg que recibieron la segunda dosis de 30 μg tuvieron fiebre leve a moderada dentro de los 7 días; los 12 participantes restantes en el grupo de nivel de dosis de 30 μg recibieron una segunda dosis de 10 μg aproximadamente 1 mes después de la primera dosis. “Los datos informados en este documento apoyan la vacunación de niños de 5 a 11 años con dos dosis de 10 μg de la vacuna BNT162b2. La evaluación de BNT162b2 en niños más pequeños está en curso”, concluye el estudio de JAMA.
Fuente: INFOBAE
